
우울증은 알츠하이머치매 환자의 절반 가량에서 동반되고 돌봄 부담을 가중시키는 중요한 증상인 만큼 알츠하이머에 동반된 우울증을 개선시키는 것은 매우 중요한 의미를 가진다.
아리바이오(이하 ‘회사’)는 지난 11월 발표한 남성 발기부전치료제 AR1001(성분명: mirodenafil)의 알츠하이머 미국 임상 2상을 분석한 후 ‘우울증상의 획기적인 개선도 놀라운 결과’라고 강조했다.
또한, 이번 답변에 앞서 회사는 지난 12월 16일에 배포한 보도자료에서도 AR1001이 ‘치매성 우울증을 개선하는 의미있는 결과’를 보였다고 발표했다.
이에, AR1001이 알츠하이머치매 환자의 우울증을 어느 정도 개선시켰는지 그리고 회사가 밝힌 바와 같이 과연 ‘우울증상을 놀라울 만큼 획기적으로 개선’시켰는지 살펴볼 필요가 있어 보인다.
이번 임상 2상은 경증 및 증등도의 알츠하이머 환자를 대상으로 AR1001을 26주간 복용했을 때의 효능과 안전성에 대한 이중맹검, 무작위배정, 대조군 연구이다. 연구는 210명의 경증 또는 중등도의 알츠하이머병 환자를 대상으로 총 26주 간 이뤄졌으며, 환자는 위약군, AR1001 10 mg 복용군, 또는 AR1001 30 mg 복용군으로 무작위 배정됐다. 위약군 환자는 추가 26주 연장시험에 선택적으로 참여했으며, 10 mg 또는 30 mg 복용군으로 재배정됐다.
연구에서 유효성을 평가하는 두 가지 일차지표는 ADAS-Cog 13 (Alzheimer's Disease Assessment Scale-Cognitive subscale 13)과 ADCS-CGIC (Alzheimer's Disease Cooperative Study-Clinical Global Impression of Change)이며, 2차지표로는 MMSE-2 (Mini-mental status examination 2), NPI (Neuropsychiatric Inventory), GDS (Geriatric Depression Scale, 노인우울척도), C-SSRS (Columbia Suicide Severity Rating Scale), QOL-AD (Quality of Life in Alzheimer's Disease) 등을 사용했다.
이 연구에서 AR1001이 알츠하이머 환자에 동반된 우울증을 획기적으로 개선시켰다는 결론을 내리기 위해서는, AR1001(10 mg 또는 30 mg)을 복용한 환자에서 26주 후의 GDS 점수로 평가한 우울증상이 위약군보다 개선됐다는 것을 통계적으로 입증해야 한다.
지난 11월 CTAD 2021 학회에서 공개된 자료에 따르면, 알츠하이머치매의 진행 정도에 따라 ‘경증 치매군’과 ‘증등도 치매군’으로 구분하고 ‘AR1001 단독 복용군’과 ‘AR1001군과 기존 알츠하이머치매 치료제 병용 복용군'으로 나누어 GDS 점수 변화의 하위그룹분석(sub-group analysis)이 이뤄졌다.
아래 도표로 표시된 분석 결과를 보면, 연구 시작 26주 후에 경증 치매군과 증등도 치매군, 그리고 단독 복용군과 병용 복용군 어느 그룹에서도 GDS 점수가 위약군보다 통계적으로 의미있게 개선됐다는 근거를 찾을 수가 없다.
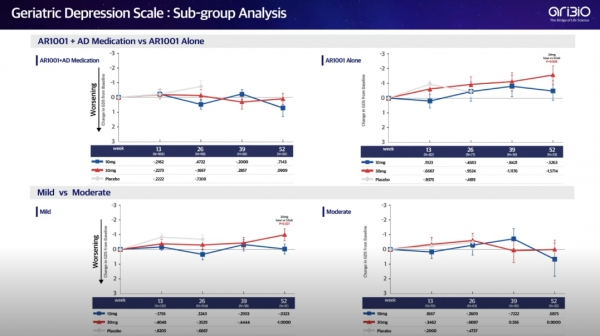
다만, 위약 대조군이 존재하지 않는 52주 후에 ‘AR1001 30 mg 단독 복용군’과 ‘AR1001 30mg을 복용한 경증 치매군’에서 위약군 대비가 아닌 연구 시작점 대비 우울증이 개선되었을 뿐이다.
AR1001 10 mg 또는 30 mg을 기존의 치매약과 병용한 경우, AR1001 10 mg 단독 복용군, AR1001 10 mg을 복용한 경증 치매군, AR1001 10 mg 또는 30 mg을 복용한 증등도 치매군에서는 통계적으로 유의미한 우울증 개선 효과를 확인할 수 없다.
위와 같이 우울증 개선효과를 평가하기 위한 GDS 점수 변화의 분석 결과를 종합해보면, AR1001이 알츠하이머치매에 동반된 우울증을 획기적으로 개선시켰다고 결론을 내릴 만한 근거는 충분치 않아 보인다.


