
중앙보훈병원 신경과 양영순 과장
아세틸엘카르니틴(ALC) 성분 제품은 국내에서 흔히 사용되는 대표적인 뇌기능개선제 중 하나지만, 그동안 효능이나 효과를 입증할만한 자료는 충분치 못했다.
약을 처방하는 대다수 의사들조차 ALC는 아세틸콜린을 증가시켜 주는 전구 물질로 알고 사용하고 있는 것이 전부인 경우가 많다.
최근 국내에서는 ALC 성분이 인지기능 개선에 효과가 있다는 것을 확인하기 위한 의미있는 연구가 진행됐으며, 그 결과가 치매학회지를 통해 공개됐다.
논문 제목은 'A Multicenter, Randomized, Double-blind, Placebo-controlled Clinical Trial for Efficacy of Acetyl-L-carnitine in Patients with Dementia Associated with Cerebrovascular Disease'.
이 연구에는 중앙보훈병원, 한양대병원, 고려대병원, 삼성의료원, 용인효자병원 등 5개 병원이 참여했다.
디멘시아뉴스는 논문 1저자로 연구를 진행한 중앙보훈병원 신경과 양영순 과장을 만나 이번 연구의 의의를 들어봤다.
ALC는 일반적으로 뇌영양제로 많이 처방하는 약이지만, 1990년대 마지막 논문이 나왔을 정도로 최신 연구가 없다. 더구나 흔히 사용되는 전문약임에도 불구하고 관련 임상 없이 약이 처방되고 있다.
양 과장는 "ALC가 막연하게 환자들에게 효과가 있을 것이라는 생각을 가지고 많은 의사들이 처방을 하고 있지만, 정말 효과가 있을 지에 대한 근거는 부족하기 때문에 그 근거를 찾기 위한 연구를 진행하게 됐다"고 말했다.
연구 대상자는 55~80세 노인으로 12개월 이내에 CT 또는 MRI로 확인된 허혈성 뇌병변이 있으며, 정신장애 진단 및 통계 매뉴얼로 진단된 치매환자였다. 또 K-MMSE 점수는 12~26점이며, 도네페질을 복용하는 환자가 대상이었다.
연구는 2개군으로 나누어 28주 동안 ALC를 복용한 환자와 복용하지 않는 군을 비교했다. ALC 복용군과 위약군은 각각 30명, 26명이었다.
주 평가 항목은 MoCA-K(한국판 몬트리올 인지평가)였으며, 두번째 평가항목을 MMSE-K(한국판 간이정신진단검사) 등으로 했다.

MoCA를 통해 평가할 수 있는 항목은 주의력, 어휘력, 추상력, 문장력 등인데, 연구 결과 ALC를 복용한 환자 군에서 언어 능력과 집중력 개선에서 의미있는 결과를 도출해 냈다.
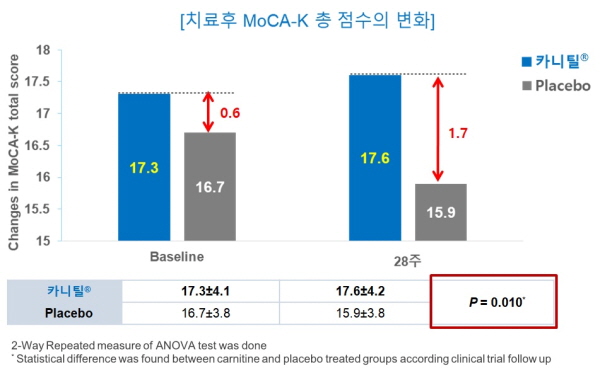
MoCA 점수로 보면 연구 초기 ALC 투여군과 위약군의 점수는 각각 17.3, 16.7로 0.6점 차이가 났다. 28주 후에는 ALC 투여군과 위약군이 각각 17.6, 15.9로 1.7점 차이가 났다. 28주 후 MoCA 점수가 1.1점 개선됐다는 결과였다.
이번 연구를 기초로 도네페질을 복용하지 않는 경도인지장애(MCI due to AD) 환자를 대상으로 한 추가 연구도 할 수 있을 것이라고 봤다. 다만 아직 해당 연구에 대한 계획은 없는 상태다.
양 과장은 "개원의들을 대상으로 한 강의를 가면 이 연구 결과를 통해 막연하게 ALC에 대한 질문을 많이 하지만 그동안 해당 약물의 기전을 얘기하는 것이 전부였다"며 "이번 논문을 통해 ALC의 효능을 정확히 말할 수 있으며, 의사들도 약에 대한 자심감을 가지고 처방할 수 있게 됐다"고 덧붙였다.
한편, 식약처는 아세틸엘카르니틴 성분 뇌기능개선제에 대해 2013년 유효성 입증을 위한 임상재평가를 지시한 바 있다.
해당 성분은 일차적 퇴행성질환과 뇌혈관질환에 의한 이차적 퇴행성질환 등 2개 적응증을 보유하고 있으며, 각각의 질환에 대한 임상재평가를 진행하고 있다. 일차적 퇴행성 질환과 이차적 퇴행성 질환에 대한 임상재평가는 각각 2019년과 2021년 종료될 예정이다.
임상재평가를 통해 두 가지 적응증에 대한 유효성을 입증하게 될 경우 해당 성분 약물 처방에 대환 신뢰는 더 높아질 것으로 기대된다.
디멘시아뉴스 최봉영 기자(bychoi@dementianews.co.kr)


