치료제 2건·진단기기 4건...상담 실적 저조

식약처가 4년째 운영 중인 치매치료제·진단기기 제품화 기술지원단의 작년 상담 실적이 신통치 않은 것으로 나타났다.
식약처와 상담이 대부분 초기 개발 단계의 업체에 집중돼 있는 것을 감안하면, 신규 개발에 대한 열기가 전보다 식었다는 것을 의미한다.
19일 식품의약품안전처에 따르면, 치매치료제·진단기기 제품화 기술지원단(이하 지원단)의 누적 상담 건수는 총 37건으로 나타났다.
2018년에 출범된 지원단은 국내 개발 중인 치매치료제와 체외진단용 의료기기의 제품화 성공률을 높이기 위해 연구개발 초기부터 허가까지 단계별로 맞춤형 기술지원을 하는 것이 주요 업무다.
지원단 출범 초기만 하더라도 상담 건수가 10건 이상이었으나, 지난해와 올해의 경우에는 상담 사례가 눈에 띄게 줄었다.
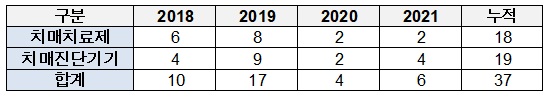
2018년 상담 건수는 10건, 2019년 17건, 2020년 4건, 2021년 6건을 기록했다.
치매치료제만 떼 놓고 보면, 2018년 6건, 2019년 8건, 2020년 2건, 2021년 2건이었다. 지난 4년간 누적 건수는 18건이었다.
치매치료제 개발을 위한 상담 건수가 줄어든 것은 신규 임상에도 반영됐다. 신규 생동시험과 임상시험은 총 18건을 허가받았으나, 대다수가 제네릭 개발에 집중됐다.
또 일부 다국적제약사가 신약 개발을 위한 임상 승인을 받았으나, 국내사의 신규 임상 허가는 저조했다.
치매진단기기의 경우 2018년 4건, 2019년 9건, 2020년 2건, 2021년 4건이었으며, 누적 건수는 19건이었다.
치매진단기기도 지원단 출범 초기에 비해 상담이 대폭 감소했다.
실제 일부 업체가 치매약이나 진단기기 개발에 나서고는 있지만, 임상 단계에 이르지 못하고 개발을 중도 포기하는 사례가 발생하고 있는 것으로 알려졌다.
치매치료제 개발을 위해 국내사뿐 아니라 많은 다국적제약사들도 대규모 투자를 이어가고 있으나, 상용화까지 이어진 제품은 손에 꼽는다.
성공보다 실패의 가능성이 큰 데다 대형 제약사들도 치매약 개발에서 성과를 못 내고 있는 만큼 꺼져가는 신약 개발의 불씨를 되살리기는 쉽지 않을 전망이다.

