KAIST–KBRI, 균일 3색 OLED 광자극 기술 개발
동물모델에서 병리·기억 기능 개선 확인…전자약 가능성 주목
한국과학기술원(KAIST) 전기 및 전자공학부 최경철 교수 연구팀과 한국뇌연구원(KBRI) 구자욱·허향숙 박사 연구팀은 청색·녹색·적색 3가지 파장을 균일하게 구현하는 OLED(Organic Light-Emitting Diode 유기발광다이오드) 기반 광자극 플랫폼을 개발하고 이를 알츠하이머 동물모델에 적용한 결과, 적색 40Hz 광자극이 병리적 지표와 기억 기능을 가장 효과적으로 개선하는 것을 확인했다고 밝혔다.
연구 결과는 재료 기반 바이오의공학 분야 국제 SCI 학술지 <ACS Biomaterials Science & Engineering> 온라인판 10월 25일 자에 게재됐다.
빛의 파장·주파수를 정밀 비교…“적색에서 가장 확실한 개선”
기존 LED 광자극은 밝기 편차, 발열, 색 균일도 문제로 파장별 효과 비교가 어려웠다. 이번에 개발된 OLED 플랫폼은 균일 조도와 낮은 발열, 소형화가 가능해 색상·주파수에 따른 생체 반응을 정밀하게 비교할 수 있는 환경을 제공한다.
초기 병기 동물모델에서는 세 파장 모두 기억력 향상과 아밀로이드베타(Aβ) 감소가 관찰됐지만, 염증 조절 효과는 적색광에서 가장 뚜렷했다.
중기 병기에서도 적색광은 Aβ 플라크 감소와 기억 기능 향상을 동시에 유도하며, 백색광 대비 병리 개선 효과가 훨씬 분명하게 나타났다.
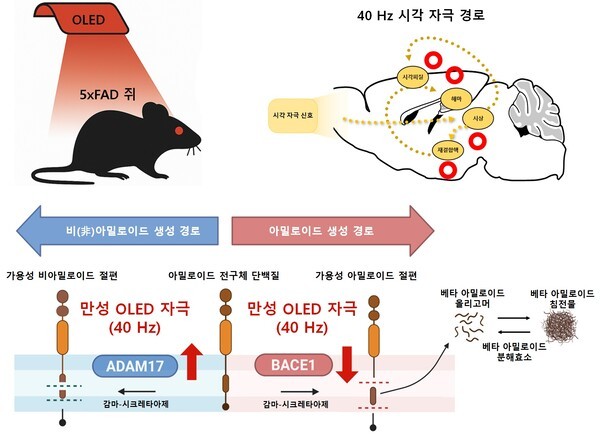
플라크 생성·분해 경로 모두 조절하는 ‘적색 40Hz’
분자 수준의 분석에서도 적색광의 선택적 효과가 확인됐다. 적색 40Hz 자극에서는 ▲플라크 분해 효소 ADAM17 증가 ▲플라크 생성 효소 BACE1 감소가 동시에 나타나는 양방향 조절 효과가 관찰됐다. 반면, 백색광은 BACE1만 감소했으며 ADAM17 증가 효과는 없었다.
또한 빛 자극 직후 활성화되는 신경표지 단백질 c-Fos 분석에서는 시각피질–시상–해마로 이어지는 기억 회로가 활성화돼 “빛이 시각 경로를 통해 인지 기능과 연결된다”는 근거도 제시됐다.
연구팀은 “적색 40Hz가 병리와 인지 기능을 함께 개선한다는 점은 비침습적 광자극 치료의 가능성을 크게 확장하는 발견”이라고 설명했다.
향후에는 자극 강도·기간·멀티모달 자극(시각·청각 결합 등)을 포함한 조건 확장과 임상 단계로의 진입이 추진된다.
‘전자약’으로 이어지는 치료 패러다임의 변화
‘전자약(electroceutical)’은 약물 대신 전기·광·자기·초음파 등 물리적 에너지로 신경회로를 조절하는 치료기술을 말한다. 심장박동기, 뇌심부자극기(DBS), 경두개자극기(TMS) 등이 대표적이다.
이번 OLED 기반 광자극 기술은 가볍고 얇아 착용이 용이하며, 발열이 거의 없고, 특정 파장과 주파수를 정밀하게 제어할 수 있어, 전자약에 적용할 수 있는 높은 확장성을 가진다.
특히 이번 연구에서 확인된 적색 40Hz의 병리 개선과 기억 개선 동시 효과는 빛이 하나의 ‘약’처럼 작용할 수 있음을 보여주는 직접적 근거다.
이는 약물 중심의 기존 접근에서 벗어나, 치매 초기·경도인지장애(MCI) 단계에서 사용할 수 있는 비약물적·비침습적 중재기술로 이어질 가능성을 열어준다.
OLED 광자극 기술은 궁극적으로 ‘몸에 부착하는 알츠하이머 전자약’으로 발전할 잠재력이 있으며, 이번 연구는 그 가능성을 실제 데이터로 입증한 초기 성과로 평가된다.
Source
Choi, K., Kim, M., Kim, N., Park, S., Koo, J., & Hur, H., et al. (2025). Color Dependence of OLED Phototherapy for Cognitive Function and Beta-Amyloid Reduction through ADAM17 and BACE1. ACS Biomaterials Science & Engineering, Online ahead of print. https://doi.org/10.1021/acsbiomaterials.5c01162

- 인지기능 개선, 비침습 뇌 자극 치료...tDCS, rTMS 무엇일까?
- 국내 연구진, 뇌질환 환자 “뇌파로 증상 정도 진단하고 맞춤치료한다”
- 4년 추적 고령자 연구, “악기 연주로 70대 뇌 노화 멈췄다”
- 코그테라, 메타기억훈련 디지털 치료기기 보건복지부 혁신의료기술 지정
- 수면 중 뇌 청소 실시간 측정…치매 조기 진단과 치료 기술 새 전기
- 혈액 단백질로 치매 예측…아주대 연구팀, AI 진단 모델 ‘PPIxGPN’ 개발
- 치매 진단 10년 앞당길 단백질 지도 나왔다…한국도 활용 가능
- [현장] KIMES 2025...차세대 융복합 의료산업 및 첨단 정밀의료 기술 한눈에
