최우선 순위 신규 투자로 ‘중개 연구 및 임상 중재’에 1억 4,800만 달러
▲구강 건강 ▲임상적으로 의미 있는 개선 ▲유전자 변이 치료 ‘주목’

미국 국립보건원(NIH)이 2026년 회계연도 기준 알츠하이머병 및 관련 치매(AD/ADRD) R&D 예산으로 39억 8,448만 5,000달러(한화 약 5조 4,906억 원)를 편성했다.
이는 전년도인 2025년 기준 예산(40억 6,706만 4,000달러)보다 2%가량 감소한 수치지만, 올해 연구비 지출 추정치(38억 7,100만 달러)보다는 약 2.9% 더 늘어난 금액이다.
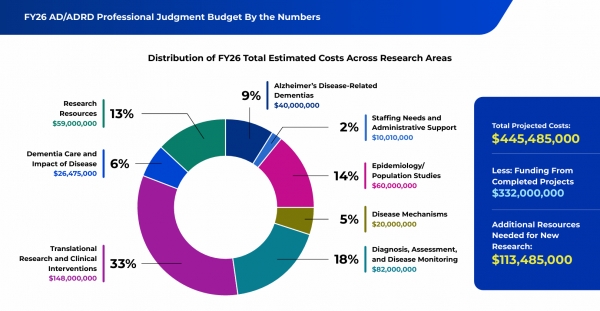
전체 예산 가운데 새로운 연구로 투입되는 투자금은 4억 4,548만 5,000달러(약 6127억 원)다. 앞서 완료된 프로젝트에서 확보한 3억 3,200만 달러를 제외할 경우 1억 1,348만 5,000달러(약 1,561억 원)가 추가로 지원되는 셈이다.
이번 연구 예산 보고서는 지난 5일(현지 시간) 알츠하이머병 연구, 치료 및 서비스 자문위원회(Advisory Council on Alzheimer's Research, Care and Services, 이하 자문위) 회의에서 공개됐다.
미국 보건복지부(HHS)는 오바마 전 대통령 재임 시절인 2011년에 마련된 국가 알츠하이머 프로젝트법(National Alzheimer's Project Act, NAPA)에 따라 중장기적인 연구 목표 달성 단계(Milestones)를 수립하고, 전문가 자문위를 통해 전체 예산안과 더불어 신규 연구를 지원하는 추가 예산안도 심의한다.
이번에 신규로 추가된 연구 예산의 투자 우선순위는 ▲중개 연구 및 임상 중재(1억 4,800만 달러) ▲진단, 평가 및 질병 모니터링(8,200만 달러) ▲역학·인구 연구(6,000만 달러) ▲연구 자료(5,900만 달러) ▲치매 치료 및 질병 영향(2,647만 5,000달러) ▲질병 메커니즘(2,000만 달러) 순이다.
특히, NIH는 이번 추가 예산 편성에서 세 가지 신규 투자 연구 분야를 주목했다.
먼저 ‘구강 건강과 인지 장애 및 치매의 위험성’이다.
보고서는 최근 구강 건강이 인지 장애와 치매 위험에 영향을 미치는 요소로 떠오르고 있다고 소개했다. 구강 건강이 나빠질수록 치매 위험이 커진다는 것이다.
NIH 연구진에 따르면, 잇몸 질환인 치주염이 치매 발병 및 사망 위험 증가와 관련이 있는 것으로 나타났다. 연구진은 이 같은 연관성에 영향을 미칠 수 있는 여러 종류의 박테리아를 확인했다. 다만 아직 구강 건강과 치매의 연관성에 대한 근본적인 메커니즘은 알려지지 않았다.
NIH는 이번 추가 투자를 통해 구강 건강과 치매 연관성에 대한 이해를 높이는 연구에 자금을 지원할 방침이다. 또 치매 위험이 크거나 치매를 앓는 사람들의 구강 건강과 위생을 개선하기 위한 효과적 행동 및 사회적 개입의 필요성을 다룰 계획이다.
또 레카네맙과 도나네맙 사례를 들면서 ‘임상적으로 의미 있는 개선’을 중요한 요소로 봤다.
보고서에 따르면, ‘임상적으로 의미 있는 개선’이란 치매 환자나 간병 파트너가 가치가 있다고 생각하는 증상 변화 또는 지연을 뜻한다.
보고서는 “2023년 7월 레카네맙, 2024년 7월 도나네맙 등 알츠하이머병의 근본적인 병리를 표적으로 하는 두 가지 약물이 미국 식품의약품청(FDA)으로부터 승인을 받았다”며 “그 외에 몇 가지 유망한 치료 옵션이 현재 임상시험에서 평가되고 있다”고 설명했다.
그러면서 “이러한 진전이 흥미롭고 고무적”이라면서도 “잠재적 치료법이 임상시험 과정과 그 이후에 ‘임상적으로 의미 있는’ 방식으로 효과적인지 여부를 측정하는 방법에 대한 새로운 도전과 의문도 드러났다”고 지적했다.
다만 치매 연구에서 개인마다 치매를 경험하는 방식이 다르다면 ‘임상적으로 의미 있는 결과’를 이해하는 데 큰 어려움이 따른다고 덧붙였다. 동반 질환, 장애 중증도, 발병 연령 등 다른 요인들의 영향을 받을 수 있다는 것이다.
이전 연구에서도 이 같은 결과에 대한 조명이 이뤄졌지만, 기억력이나 기능, 독립성, 건강 등 중요한 연구 결과를 추가로 탐색해야 할 필요성이 있다고 제시했다.
NIH는 인지 기능, 신체 건강, 사회 및 정서적 웰빙 등 여러 양상에서 치매 영향을 받는 사람들에게 가장 중요한 결과를 공평하게 파악하기 위한 ‘사람 중심의 협력적 연구’에 자금을 지원한다고 밝혔다.
지원금은 치매 환자와 간병 파트너의 주요 우선순위를 반영한 새로운 연구 도구 및 평가의 개발과 검증에 쓰일 예정이다.
한편, 이 연구가 아두헬름, 레켐비, 키선라 등과 같은 항아밀로이드 항체 치료제 임상시험에서의 지속적인 노력을 기반으로 하고 이를 보완하기 위한 것이라고도 강조했다.
마지막으로 유전자 변이를 활용한 알츠하이머병 및 관련 치매 치료제 개발에 주안점을 뒀다.
최근 몇 년간 NIH의 지원을 받는 알츠하이머병 연구자들은 RELN 유전자 변이(RELN-COLBOS)와 APOE 유전자 변이(APOE3 Christchurch, APOE3ch)를 이용한 알츠하이머병 치료제 개발이 새로운 길을 열 가능성이 크다고 전망했다.
희귀 변이가 어떻게 치매 예방을 하는지 이해하면 효과적인 치매 예방 중재를 개발할 수 있다는 것이다. NIH는 APOE3ch에서 영감을 얻은 항체가 이미 연구되고 있다고 언급했다. 하지만 유전자와 치매 예방 메커니즘을 완전하게 이해하기에는 여전히 한계가 있다고 봤다.
NIH는 연령, 유전적 위험, 심혈관 위험 요소, 특정 치매 바이오마커 존재 등 다양한 유형의 인구 집단에서 유전자-환경 상호작용이 인지 회복력으로 이어지는 분자 메커니즘을 심층적으로 이해하는 연구에 추가로 투자할 예정이다.
이 연구가 질병 예방을 위한 회복탄력성 기반 치료제 개발과 이와 관련한 신규 바이오마커 개발에 도움이 될 것으로 기대했다.
모니카 베르타뇰리(Monica M. Bertagnolli) NIH 원장은 공식 메시지를 통해 “알츠하이머병 및 관련 치매 연구는 지난 몇 년 동안 놀라운 속도로 발전해 왔다”며 “이러한 동력을 바탕으로 치매 환자와 그 가족을 위한 연구 혁신을 가속하기 위해 최선을 다하고 있다”고 말했다.
Primary Source
Fiscal Year 2026 NIH Professional Judgment Budget for Alzheimer’s Disease and Related Dementias Research: Advancing Progress in Dementia Research

- WHO, 정신건강분야 투자 5% 권고 했지만 우리나라 1.9% 불과
- "구강 건강 나쁠수록 인지기능 저하" 의치 착용 연관성 포착
- 23년 보건의료 연구개발 예산 1조 4,690억 원 지원
- 英 연구진 “레켐비·키선라, 효과 ‘낮고’ 부작용 ‘빈번’”
- 랜싯 치매 위원회가 본 ‘항아밀로이드 항체 치료제 논란’
- [기자의 눈] 레카네맙은 과연 최소한의 ‘임상적 의의’를 충족시키는가?
- 美 연구팀 “알츠하이머병 늦추는 희귀 변이 유전자 발견”
- “차라리 몰랐으면” … 'APOE4' 유발인자 발견, 충격으로 공포의 나날
- 한국인 20%가 보유한 ‘APOE4 동형접합형’과 알츠하이머병 징후
- |치매극복연구개발사업| 치매 신약 개발, 집중 지원 국내 기업은?
- 일라이 릴리, 도나네맙 후속 '타우 표적 알츠하이머 치료제' 실패
- “2020~50년, 세계 152개국 치매 관련 경제적 비용 ‘1경 9,729조원’”
- 빌 게이츠, ‘알츠하이머병 연구’ 美 인디애나의대 방문 '주목'
- 中, G20 국가 중 ‘치매 부담’ 가장 높아...“30년간 치매 환자 322%↑”
- 내년 치매안심센터 예산 대폭 줄어...R&D·시설 투자는 소폭 증가
